
试验设计 在补充有短链脂肪酸(SCFA)的快速厌氧菌肉汤(FAB)中对F. prausnitzii进行体外培养,在10 ml FAB+SCFA培养基中添加0.5% (w/v %)的XOS或不添加XOS,培养19、20.5、22和23.33小时后,用MultiskanFC光度计测定XOS对两种市售的F. prausnitzii菌株(ATCC-27766和DSM A2-165)的影响。 采用10~12周龄的雄性Wistar大鼠作为试验研究对象,将大鼠随机分为4组,HFD组(高脂饮食组,60%的能量来自脂肪)、HFD+XOS组(补充0.12% XOS的HFD组)、LFD组(对照组=低脂饮食组,10%的能量来自脂肪)和LFD+XOS组(补充0.12% XOS的LFD组),每组10只,自由饮食,干预12周,研究期间,每周进行体重、体成分和食物摄入量测定,通过呼吸气体中的氧气和二氧化碳,间接测量代谢能力。 干预结束,穿刺抽血安乐死,采用KONELAB 20XTi分析仪测定血清葡萄糖、甘油三酯、游离脂肪酸、甘油、胆固醇、低密度脂蛋白胆固醇、高密度脂蛋白胆固醇、天冬氨酸转氨酶(AST)和丙氨酸转氨酶(ALT)水平;采用IMMULITE分析仪测定血清胰岛素;采用ELISA试剂盒测定细胞因子;收集肝脏、肠道组织,进行组织学检查;收集近端结肠和盲肠内容物,提取DNA,对F. prausnitzii进行实时荧光定量PCR;通过16S rRNA基因测序,进行细菌菌落分析,确定细菌组成;提取盲肠代谢物,进行鉴定与分析;测定肝脏脂肪含量及3-羟酰基辅酶A脱氢酶活性;通过高分辨率呼吸仪测定肝脏线粒体功能分析肝脏糖代谢率;提取肝脏和脂肪组织的总RNA,转录为cDNA,进行实时PCR分析。 试验结果 (1)XOS促进F. prausnitzii的生长 如图1所示,DSM A5-165菌株在对照组和XOS处理组之间的差异是显著的(P<0.05),但在ATCC-27766菌株中没有差异。在大鼠中,经过12周的XOS补充,与不添加XOS的HFD和LFD相比,F. prausnitzii的丰度显著增加。
(2)通过增强脂肪和葡萄糖代谢而降低肝脏脂肪含量 如图2所示,与LFD组相比,HFD组增加了甘油三酯水平(p<0.001),与HFD组相比,HFD+XOS组的甘油三酯水平降低(F(1,0.8)=6.5,p=0.017),与LFD组相比,LFD+XOS组则增加了肝脏甘油三酯。在组间比较中,只有LFD+XOS的肝脏胆固醇含量显著高于LFD(p=0.015),表明XOS对总肝脏胆固醇有交互作用(p=0.001)。
如图3所示,XOS提高了β-HAD在HFD组中的肝脏活性(F(1,36)=4.5,p=0.041),HFD组降低了最大电子运输量(p=0.034),还降低了理论上可用于氧化磷酸化的最大电子传递能力(p=0.023),以及通过复合物I(p=0.019)和复合物I和II(p=0.013)的氧化磷酸化之外的储备电子传递能力。补充XOS似乎改善了HFD组对线粒体呼吸的影响,与HFD组相比,HFD+XOS组增加了通过复合物I的电子流产生ATP的呼吸能力(p=0.023),并改善了通过复合物I和氧化磷酸化的电子传递耦合(p=0.041)。
如图4所示,HFD组降低了SCD1(饮食的影响:F(1,36)=97.5,p<0.001)和DGAT2(饮食的影响:F(1,35)=8.7,p=0.006)的肝脏mRNA表达,但XOS对其没有影响。
(3)XOS不影响肠道微生物群的多样性,但会改变三个微生物属的相对丰度 如图5所示,XOS并不影响结肠或盲肠肠道微生物群的α-多样性(图5a)或β-多样性。
如图6所示,在属的水平上,HFD+XOS组中Dubosiella和Christensenellaceae的未培养成员最低,普雷沃氏菌科NK3B31组最高(所有p=0.01)。
(4)XOS改善了HFD诱导的肠道损伤和近端结肠的炎症标志物,但不影响肠道Tjp1(紧密连接蛋白)、肝脏IL1β mRNA或全身性炎症的发生 如图7所示,在近端结肠的组织病理学检查中,发现饮食和XOS对表面上皮损伤(p<0.001)、杯状细胞增生(p=0.001)、隐窝长度变形(p<0.001)和损伤评分(F(1,35)=90.4,p<0.001)有交互影响,XOS减少了HFD组引起的上皮损伤,而在LFD上,XOS增加了损伤(P<0.001),还增加了单核细胞聚集,即白细胞对固有层的浸润(p=0.021),但对固有层的淋巴细胞聚集,即隐窝结节或大颗粒的淋巴细胞没有影响。
如图9所示,TNFα低于检测限,即在HFD组中,<2.72 pg/mL,在LFD组的10只大鼠中,只有3只被检测到,饮食对TNFα的影响无法确定,与LFD组相比,HFD降低了抗炎性IL-10的血清水平(F(1,33)=18.0,P<0.001),HFD+XOS组变化不大,没有发现饮食对mRNA表达的影响。
(5)HFD对盲肠SCFA谱有有害影响,在HFD中,XOS降低盲肠异戊酸和酪氨酸水平 如表1所示,与LFD组相比,HFD组盲肠中SCFAs的含量较低。 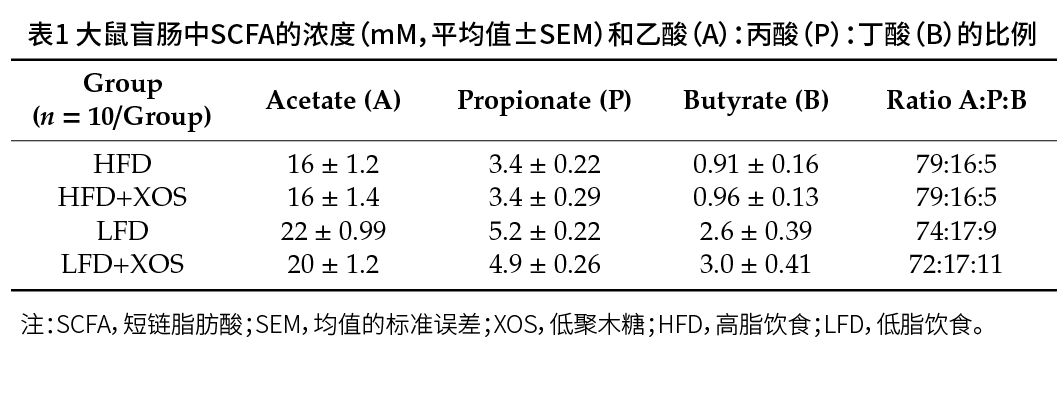 如图10所示,XOS降低了盲肠酪氨酸的水平(F(1,36)=7.7,P=0.009);XOS和饮食对异戊酸有交互作用(F(1,36)=6.0,p=0.012),在HFD组中,XOS对其有显著的降低作用(F(1,36)=8.2,p=0.007);包括SCFAs在内的几种盲肠代谢物与肝脏甘油三酯的含量呈负相关,已知能促进氧化代谢的代谢物,如烟酸、丁酸和2-氧代戊二酸,与肝脏氧化磷酸化呈正相关,与甘油三酯含量呈负相关。
(6)HFD减少了大鼠的能量消耗,而饮食和XOS对能量消耗有交互影响 如图11所示,HFD减少了平均能量消耗(饮食的主效应:白天,p<0.001;夜间,p<0.001),XOS和饮食对夜间最低静息能量消耗有交互影响(p=0.008),白天的趋势类似(p=0.071);在夜间,HFD降低了静息能量消耗,但XOS增强了它,而在LFD组上,XOS减少了静息能量消耗,与HFD组相比,LFD组在30分钟内有较高的最低昼夜能量消耗(P=0.001);在夜间,LFD组的平均能量消耗比HFD高(P=0.01);在白天(p<0.001)和夜间(p=0.001),LFD组的平均CO2产生量比HFD组高。HFD减少了夜间(p<0.001)和白天(164.7,p<0.001)的CO2产生;饮食对所有测量的昼夜RQ值有显著影响,LFD组的RQ值高于HFD组;XOS和饮食的交互作用对白天和夜间的RQ值有显著影响(所有的P<0.001)。
(7)XOS不影响典型的非酒精性脂肪肝相关标志物或身体成分,但对能量摄入有交互影响 如表2所示,与LFD组相比,HFD组增加了血清甘油三酯、AST和ALT的水平,HFD还倾向于增加游离脂肪酸(F(1,36)=3.8,p=0.059),而XOS倾向于增加甘油三酯(F(1,35)=3.2,p=0.083)。
如图12所示,饮食或XOS对肠系膜脂肪组织中脂联素mRNA的表达没有主要影响,但在LFD上,XOS增加了它的表达(F(1,34)=4.6,p=0.04),瘦素不能从肠系膜脂肪组织中准确地检测出来;在附睾脂肪组织中,饮食而不是XOS对瘦素(F(1,36)=25.5,p<0.001)和AdipoQ(F(1,36)=8.9,p=0.005)mRNA的表达有影响,HFD使两者的表达减少。
试验结论 总之,本文研究了XOS对高脂饮食诱导的大鼠肝脏脂肪变性的影响。研究发现,XOS能够增加肠道微生物群中F. prausnitzii的丰度,且不影响肠道微生物群的多样性,但会改变三个微生物属的相对丰度,并通过增强肝脏β-氧化和线粒体呼吸来改善肝脏脂肪变性。尽管XOS对整体肠道微生物群的影响较小,但其在HFD组中显著降低了肝脏中的甘油三酯含量,并提高了β-HAD的活性,从而促进了脂肪酸的氧化。此外,XOS还改善了HFD引起的结肠损伤和炎症标志物,但并未影响肠道紧密连接蛋白Tjp1的表达。以上结果表明,XOS可以通过改善肝脏氧化代谢和影响肠道菌群来改善非酒精性脂肪肝。 参考资料: Lensu S, Pariyani R, Mäkinen E, et al. Prebiotic Xylo-Oligosaccharides Ameliorate High-Fat-Diet-Induced Hepatic Steatosis in Rats[J].Nutrients. 2020, 12(11):3225. |